*仅供医学专科东说念主士阅读参考
转头2024年度ADC药物在规模的前沿进展。
抗体药物偶联物(ADC)由单克隆抗体、细胞毒性载药以及相接子偶联而成,兼具抗体的靶向特异性和载药的高毒性,权贵提高抗诊治的获益风险比,是频年来肿瘤精确诊治的前沿策动标的之一。靶向HER2的ADC药物的问世领先开启了胃癌ADC药物诊治的新时期。另外,Claudin18.2、TROP2等均在胃癌患者中过抒发,使其成为ADC研发赛说念的热点靶点。2024年,多项聚焦于HER2、Claudin18.2、TROP2等靶点的ADC药物的临床策动均赢得了令东说念主防止标效果,不仅为晚期胃癌患者带来了新的但愿,也为改日的策动指明了新的标的。值此辞旧迎新之际,一元复始之时,医学界肿瘤频说念特邀浙江大学医学院附属邵逸夫病院潘宏铭教训转头2024年度ADC药物在胃癌诊治规模的紧迫进展,以启迪临床扩展。
HER2篇
德曲妥珠单抗得手在中国获批上市,丰富HER2阳性晚期胃癌后线诊治选拔
自曲妥珠单抗在HER2阳性晚期胃癌中赢得得手以来,近十余年HER2一直是胃癌临床策动的经典靶点。关联词,胃癌的抗HER2诊治探索历程颇为鬈曲,在中赢得权贵获益的双靶诊治决策、小分子酪氨酸激酶禁锢剂、传统ADC药物等在胃癌的策动均折戟。直到新一代ADC药物(如德曲妥珠单抗、维迪西妥单抗)的出现才为HER2阳性晚期胃癌的后线诊治带来新的突破。如DESTINY-Gastric01策动中,德曲妥珠单抗后线诊治比拟化疗将HER2阳性晚期胃癌患者的中位总糊口期(OS)延迟至1年以上(12.5个月 vs 8.4个月,P=0.01,HR=0.59),梗阻了HER2阳性晚期胃癌后线诊治的糊口瓶颈 [1] 。随后开展的DESTINY-Gastric02策动进一步证实了德曲妥珠单抗在西方东说念主群的权贵疗效和安全性 [2] 。
DESTINY-Gastric06策动则动作中国桥接注册磨练,纳入既往给与过至少两种诊治决策(包括氟尿嘧啶和铂类药物)的HER2阳性晚期胃癌中国患者,进一步评估德曲妥珠单抗的疗效和安全性。令东说念主慷慨的是,2024年ESMO ASIA公布的最终分析,DESTINY-Gastric06策动赢得了与DESTINY-Gastric01一致的临床获益,尽管入组患者基线特征比拟DESTINY-Gastric01策动更差,且受到COVID-19影响。
规矩2023年6月16日,95例意向诊治患者入组,其中73例经中心现实室评估为HER2阳性(IHC 3+或IHC 2+/IHC+)纳入全分析集(FAS)。经中心证明的HER2阳性(IHC 3+和IHC2+/ISH-)晚期胃癌患者中,删除4例因COVID-19损失的病例后,明锐性分析的中位OS达12.4个月;孤苦中心审查(ICR)证明的中位缓解合手续时辰(DoR)为6.7个月,中位无进展糊口期(PFS)为5.7个月,客不雅缓解率(ORR)为28.8%,ICR证明的HER2 IHC 3+患者ORR为32.1%,ICR证明的HER2 IHC 2+/ISH+患者ORR为20.0%,策动者(INV)证明的ORR为37.0% [3] 。
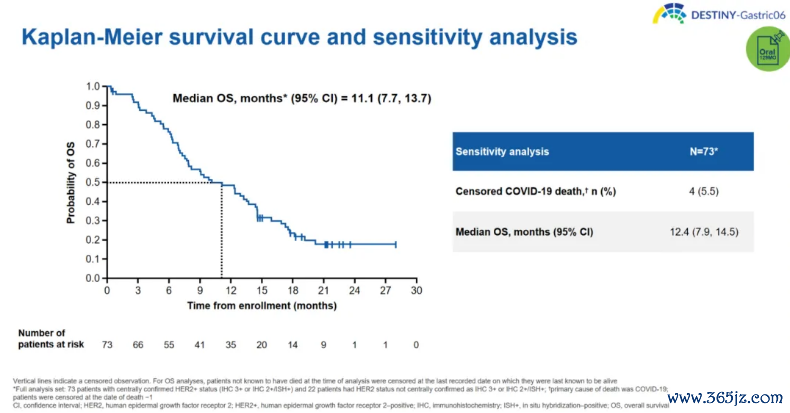
图1. DESTINY-Gastric06策动的OS终结
DESTINY-Gastric系列策动效果共同证实德曲妥珠单抗在不同种族东说念主群HER2阳性晚期胃癌真实切疗效。基于这些出色阐发,德曲妥珠单抗如故得手在日本、韩国、泰西、中国等国度和地区得手获批HER2阳性晚期胃癌适合证。当今,德曲妥珠单抗被《CSCO胃癌诊疗指南(2024)》动作HER2阳性晚期胃癌三线及三线以上诊治的III级保举(2A类凭证),同期亦然好意思国临床肿瘤学会(ASCO)、好意思国国立概述癌症集合(NCCN)、欧洲肿瘤内科学会(ESMO)干系指南中当今独一保举用于HER2阳性晚期胃癌≥二线诊治的ADC药物。
放眼大家,德曲妥珠单抗通过DAR高达8的优化缱绻,梗阻了最优DAR为2-4的传统不雅念;而拓扑异构酶I禁锢剂DXd的使用突破了微管禁锢剂抗肿瘤谱窄小的瓶颈,使得晚期胃癌的诊治投入ADC时期。聚焦国内,维迪西妥单抗的出现从头界说了胃癌HER2阳性,由以往的IHC3+或FISH阳性拓展到IHC 2+/3+,开启了国内ADC药物诊治晚期胃癌的序幕。
最近一年中,多种国产ADC药物,如FS-1502、GQ1005、IBI354等,也在HER2阳性晚期胃癌经治患者中展现了令东说念主期待的抗肿瘤疗效。
一项洞开标签、多中心、两个部队的II期策动高慢,在既往给与≥1种诊治决策、HER2阳性(IHC 3+或2+/FISH+)晚期胃癌患者中,FS-1502≥3线诊治(部队1)的ORR为37.5%,中位PFS和OS永别为4.3个月和10.0个月。FS-1502二线诊治的ORR为52.6%,中位PFS和OS永别为4.4个月和14.6个月 [4] 。
GQ1005的初次东说念主体磨练中纳入了26名HER2抒发(IHC2+/3+)胃癌患者,14例给与过曲妥珠单抗诊治,6例给与了其他HER2 ADC诊治,4例给与了HER2 TKIs诊治,GQ1005后线诊治的ORR、疾病遏抑率(DCR)和6个月PFS率永别为33.3%、80.0%和70.0% [5] 。
一项多中心、I期策动中阐发了IBI354在HER2抒发晚期胃肠癌(结直肠癌、胆说念癌、胃癌以过火他胃肠癌)患者的安全性和灵验性。共纳入34例患者,IBI354后线诊治的ORR为55.9%,DCR为91.2% [6] 。
改日,跟着对HER2阳性胃癌生物学特质的深远结伴,以及对ADC药物作用机制过火优化决策的进一步探索,咱们多情理敬佩,ADC药物将在胃癌诊治规模融会愈加紧迫的作用,为患者带来更多的糊口但愿和生活质料的升迁。
ADC伙同诊治战术为HER2阳性晚期胃癌开辟新的诊治长进
一方面,后线诊治赢得的权贵得手进一步激动着ADC药物在更前哨、更粗犷东说念主群的探索;另一方面,基于KEYNOTE-811策动(2024 ESMO公布的最终分析高慢,跟着中位随访时辰延迟,全东说念主群OS获益保合手,达到了预设的权贵性界限;但在CPS<1东说念主群中,帕博利珠单抗+曲妥珠单抗+化疗仍然无法带来更多获益[7]),免疫诊治伙同靶向及化疗如故成为HER2阳性晚期胃癌的圭臬一线诊治决策,为靶免化伙同决策的前哨愚弄带来更多信心。2024年度多项聚焦于ADC药物伙同化疗±免疫决策一线用于HER2阳性晚期胃癌的临床策动赢得了令东说念主期待的策动效果。
Ib/II期DESTINY-Gastric03策动则评估了德曲妥珠单抗单药或伙同决策的安全性和初步抗肿瘤活性。策动中患者入组后永别给与6种诊治决策:德曲妥珠单抗单药(6.4mg)、德曲妥珠单抗(6.4mg)+5-FU/卡培他滨、德曲妥珠单抗(6.4mg)+5-FU/卡培他滨+帕博利珠单抗、德曲妥珠单抗(6.4mg)+帕博利珠单抗、德曲妥珠单抗(5.4mg)+5-FU/卡培他滨+帕博利珠单抗,以及圭臬诊治(曲妥珠单抗+5-FU/卡培他滨+顺铂/奥沙利铂)[8]。DESTINY-Gastric03策动的终结将为为后续III期策动提供紧迫的参考依据。
此外,根据2024 ASCO GI大会公布的最新策动缱绻,维迪西妥单抗伙同特瑞普利单抗及化疗/曲妥珠单抗一线诊治的II/III期策动正在开展中;DESTINY-Gastric03策动决策的第二部分新增一个诊治臂,并增多了第三部分,将评估德曲妥珠单抗伙同氟尿嘧啶类和Volrustomig(MEDI5752,一种PD-1/CTLA-4双特异性抗体)用于HER2阳性和HER2低抒发(IHC 2+/ISH−或IHC 1+)晚期胃癌患者的疗效和安全性。期待更多策动效果的公布进一步激动ADC伙同决策在更早线胃癌患者的临床愚弄,为HER2阳性乃至HER2低抒发晚期胃癌患者开辟更为宽绰的诊治说念路。
CLDN18.2
多种CLDN18.2ADC药物断然入局,或将为晚期胃癌患者增多新的诊治选拔
CLDN18.2是胃癌规模继HER2之后的又一“明星”靶点,往时情况下,接续埋藏在胃黏膜中,抒发水平有限。 但在恶性肿瘤发生后,肿瘤细胞名义的CLDN18.2表位暴透露来,成为特定诊治靶点。 当今,单克隆抗体、CAR-T细胞、双特异性抗体和ADC四大类药物在CLDN18.2研发赛说念热烈角逐。 单抗Zolbetuximab如故在日本获批HER2阴性、CLDN18.2阳性晚期/复发胃癌适合症,同期多款单抗也投入III期临床阶段; 而CAR-T细胞及双特异性抗体的研发仍处于早期阶段; CLDN18.2 ADC药物的研发也投入了III期临床阶段。
CMG901(AZD0901)是一种潜在同类首创、靶向CLDN18.2的ADC药物,由东说念主源化CLDN18.2抗体通过可裂解相接子与单甲基auristatin E(MMAE)偶联而成。此前在2023年ASCO GI大会和11月的整体大会系列会议中如故公布过I期策动中晚期胃癌患者的疗效终结和安全性。2024年ASCO大会的整体大会系列会议进一步更新了该策动终结,2.2mg/kg、2.6mg/kg、3.0mg/kg三个剂量组的证明ORR永别为48%、24%和38%;中位PFS永别为4.8个月、3.3个月和9.9个月;中位OS永别为11.8个月、11.5个月和11.1个月,进一步展现了CMG901(AZD0901)在CLDN18.2高抒发晚期经治胃癌患者的超卓疗效,况且跟着随访时辰延迟,未不雅察到新的安全性信号[9]。
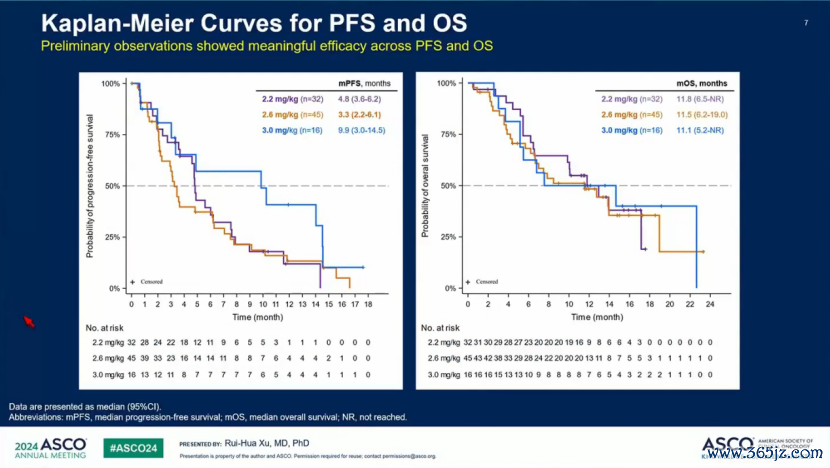
图3. CMG901用于晚期经治胃癌患者的PFS和OS终结
2024年ASCO大会中还公布了CLDN18.2 ADC药物ATG-022和LM-302的干系策动终结[10,11]。
一项针对晚期实体瘤患者的I期、多中心、洞开标签策动高慢,纳入7例胃癌患者,3例证明为CLDN18.2阳性。1例患者在ATG-022 0.9mg/kg剂量下保管疾病沉稳(SD),肿瘤收缩杰出6个月(仍在给与诊治);1例患者(CLDN18.2抒发待详情)在1.8mg/kg剂量下不雅察到部分缓解(PR);在2.4 mg/kg剂量下,CLDN18.2阴性胃癌患者中不雅察到皆备缓解(CR)。
一项包括剂量递加和剂量扩展阶段I/II期策动高慢,规矩2023年11月15日,共纳入36例既往给与过至少两种或以上其他疗法的晚期胃癌患者,LM-302诊治后不雅察到11例PR和16例SD,ORR为30.6%,DCR为75.0%。中位PFS为7.16个月。中位OS未达到,6个月OS率为95.0%。
SHR-A1904由针对CLDN18.2的IgG1单抗、可裂解相接子和拓扑异构酶I禁锢剂构成。2024年ESMO大会公布的一项I期策动高慢,在CLDN18.2阳性晚期胃癌经治患者中,SHR-A19041 6.0 mg/kg剂量组的ORR和DCR永别为55.6%和88.9%;8.0mg/kg剂量组的ORR和DCR永别为36.7%和86.7%。安全性方面,SHR-A1904高慢出细腻的耐受性,并未达到最大耐受剂量(MTD)[12]。
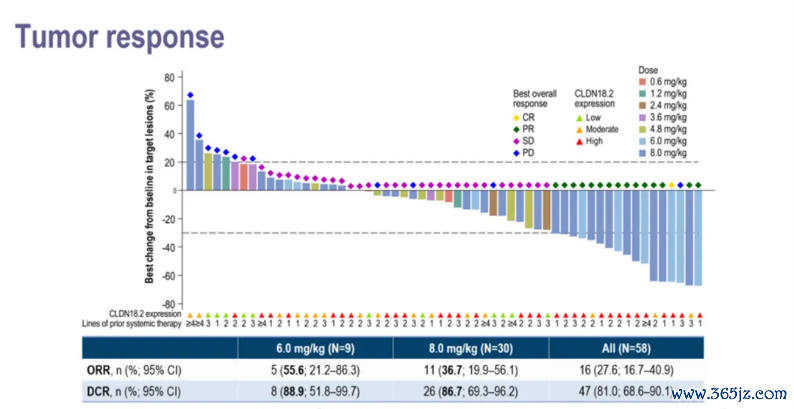
图4. SHR-A1904用于晚期经治胃癌患者的肿瘤缓解情况
2024年ESMO GI大会公布了IBI343诊治晚期胃癌的I期策动终结。规矩2024年1月15日,共纳入159例患者。规矩2024年3月29日,共有89例CLDN18.2中度至高度抒发(通过IHC检测,≥40%肿瘤细胞膜染色强度≥2+),ORR为32.6%,DCR为80.9%[13]。
在CLDN18.2(2+/3+≥40%)患者中,6mg/kg剂量组的ORR和DCR永别为31.2%和89.6%,中位PFS为5.6个月;8mg/kg剂量组永别为41.4%、82.8%和5.5个月。
在CLDN18.2(2+/3+ ≥75%)的患者中,6 mg/kg剂量组的ORR和DCR永别为36.7%和93.3%,中位PFS为6.8个月;8 mg/kg剂量组永别为47.1%、88.2%和5.5个月。
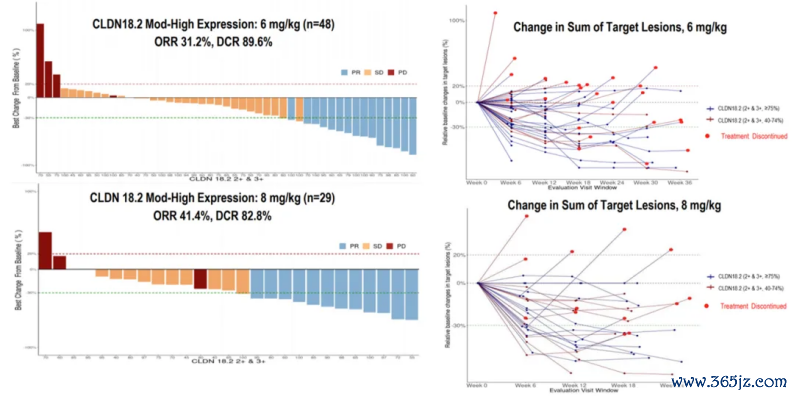
图5. IBI343诊治晚期胃癌的肿瘤缓解情况
总之,CLDN18.2靶点的成药性如故过程Zolbetuximab的考证,有望成为胃癌第二个精确诊治靶点。当今,多种CLDN18.2 ADC药物在晚期胃癌中展现了较好的灵验性和安全性,敬佩跟着III期临床策动终结的公布,将为晚期胃癌患者带来更强效的诊治选拔,进一步改善胃癌患者的糊口结局。
TROP2篇
TROP2在多种实体瘤中粗犷抒发,与不良预后缜密干系,频年来已成为ADC药物研发的热点靶点。2024年AACR年会中公布了TROP2 ADC药物芦康沙妥珠单抗用于晚期经治胃癌患者的II期拓展策动效果。KL264-01策动共纳入48例患者入组,中位随访时辰为14.2个月。其中,半数患者既往给与过一线诊治,另一半患者既往给与过≥2线诊治;83.3%的患者曾给与过PD-1/PD-L1禁锢剂诊治。终结高慢,芦康沙妥珠单抗单药诊治的ORR为22.0%,DCR达80.5%,中位DoR为7.5个月 [14] 。这些策动效果初步考证了芦康沙妥珠单抗用于晚期经治胃癌患者的权贵疗效。
总结
跟着胃癌诊治规模ADC药物的不断透露,不同靶点ADC药物研发赛说念的竞争变得愈发热烈。HER2 ADC药物如故引颈胃癌规模投入ADC药物诊治的新时期,而对于HER2 ADC药物伙同诊治战术的临床策动也在不断深远,预期将进一步改换胃癌的诊治形式。除了HER2、CLDN18.2也成为胃癌诊治中一个充满但愿的靶点,多款针对CLDN18.2的ADC药物在晚期胃癌诊治中展现出积极的探索效果,预期大要为晚期胃癌的临床诊治提供更多选拔。跟着对肿瘤生物学特质的进一步意志,以及药物缱绻和制造技巧的不断向上,咱们敬佩,ADC药物将在胃癌诊治规模饰演越来越要津的扮装。2024年的年度清点只是起先,只是是一个启动,改日还有更多值得期待的进展和突破。
巨匠简介

潘宏铭 教训
浙江大学医学院附属邵逸夫病院
浙江大学求是特聘大夫、博士生导师,肿瘤内科学科带头东说念主
国度合理用药巨匠委员会委员
国度卫健委继教中心肿瘤学概述组组长
中国抗癌协会肿瘤靶向诊治专委会候任主任委员
中国临床肿瘤学会常务理事
CSCO肿瘤养分诊治巨匠委员会主任委员
CSCO接济和康复巨匠委员会候任主任委员
浙江省肿瘤靶向诊治技巧设备中心主任
浙江省抗癌协会东说念主工智能肿瘤诊疗专委会
发表中英论文120余篇,主合手和参加临床磨练260多项,主编《肿瘤化疗的毒副反馈和防治》、《肿瘤内科诊治战术》和《肿瘤内科合理诊治和用药手段》等,
主合手制订《中国肿瘤患者养分诊治指南》、《消化说念肿瘤合理用药指南》等,
主合手国度紧要新药创制专项、国度当然科学基金和浙江省紧要科技专项等省部级以上课题10多项。
精彩资讯等你来
参考文件:
[1]Shitara K, Bang YJ, Iwasa S, et al. Trastuzumab Deruxtecan in Previously Treated HER2-Positive Gastric Cancer. N Engl J Med. 2020 Jun 18;382(25):2419-2430.
[2]Van Cutsem E, di Bartolomeo M, Smyth E, et al. Trastuzumab deruxtecan in patients in the USA and Europe with HER2-positive advanced gastric or gastroesophageal junction cancer with disease progression on or after a trastuzumab-containing regimen (DESTINY-Gastric02): primary and updated analyses from a single-arm, phase 2 study. Lancet Oncol. 2023 Jun 14:S1470-2045(23)00215-2.
[3]Shen L, Chen P, Lu J, et al.Trastuzumab deruxtecan in Chinese patients with previously treated HER2-positive locally advanced/metastatic gastric or gastroesophageal junction adenocarcinoma: DESTINY-Gastric06 final analysis. 2024 ESMO Asia.129MO.
[4]Pan HM, Yuan XL, Zheng Y, et al. FS-1502 in patients with HER2 high expression, locally advanced or metastatic gastric or gastroesophageal junction adenocarcinoma: An open-label, multicenter, phase II study. 2024 ASCO.e15000.
[5]Deng T, Sun Y, Wang B, et al. Preliminary results of GQ1005 in metastatic HER2-low expressing breast cancer and HER2 positive gastric cancer. 2024 ESMO. 644P.
[6]Safety and efficacy of IBI354 (anti-HER2 ADC) in patients (pts) with advanced gastrointestinal (GI) cancers: Results from a phase I study. 2024 ESMO. 576P.
[7]YELENA Y J, AKIHITO K, YUXIAN B, et al. Final overall survival for the phase III, KEYNOTE-811 study of pembrolizumab plus trastuzumab and chemotherapy for HER2+ advanced, unresectable or metastatic G/GEJ adenocarcinoma. 2024 ESMO. 1400O.
[8]Trastuzumab deruxtecan (T-DXd) monotherapy and combinations in patients (pts) with advanced/metastatic HER2-positive (HER2+) esophageal, gastric or gastroesophageal junction adenocarcinoma (GEJA): DESTINY-Gastric03 (DG-03).2024ESMO.1401O.
[9]Xu R, et al. Updates on Abstract 434420: A Phase 1 Trial of Claudin 18.2-Specific Antibody-Drug Conjugate CMG901 in Patients with Advanced Gastric/Gastroesophageal Junction Cancer. 2024 ASCO Plenary Series.
[10]Bishnoi S, Cao D, Mendis SR , et al. An open-label, multicenter, phase I study of ATG-022 in patients with advanced/metastatic solid tumors (CLINCH). 2024 ASCO. 3032.
[11]Bai Chunmei, Xue JL, Zheng Y, et al. A phase 1/2 study of LM-302, an anti-claudin 18.2 (CLDN18.2) antibody-drug conjugate in patients with advanced gastric/gastroesophageal junction cancer. 2024 ASCO. 3028.
[12]Xu RH, Ruan D, Luo S, et al. CLDN18.2 targeted antibody-drug conjugate (ADC), SHR-A1904, in patients (pts) with gastric/gastroesophageal junction cancer (GC/GEJC): A phase I study. 2024 ESMO.609O.
[13]Jia Jenny Liu. Anti-claudin 18.2 (CLDN18.2) antibody-drug conjugate (ADC) IBI343 in patients (pts) with solid tumors and gastric/gastro-esophageal junction adenocarcinoma (G/GEJ AC): A phase I study. 2024 ESMO GI. 396MO.
[14]Rodon J,Wainberg ZA,Zhang MJ, et al. Preliminary efficacy and safety results of anti-TROP2 ADC SKB264 (MK-2870) in patients (pts) with previously treated advanced gastric (G) or gastroesophageal junction (GEJ) cancer from a Phase 2 study.2024 AACR. CT038.
*此文仅用于向医疗卫生专科东说念主士提供科学信息,不代表平台态度。